- Soumission de LUMEVOQ® en Europe prévue en septembre 2020
Paris, France, mardi 21 juillet 2020, 7h30 CEST – GenSight Biologics (Euronext : SIGHT, ISIN : FR0013183985, éligible PEA-PME), société biopharmaceutique dédiée à la découverte et au développement de thérapies géniques innovantes pour le traitement des maladies neurodégénératives de la rétine et du système nerveux central, publie aujourd’hui les résultats finaux de l’étude d’histoire naturelle REALITY, qui viennent à nouveau confirmer le mauvais pronostic pour la très grande majorité des patients atteints de Neuropathie Optique Héréditaire de Leber (NOHL) associée à la mutation du gène mitochondrial ND4.
« Les résultats de REALITY renforcent notre conviction que les observations de REVERSE, RESCUE et la première analyse de CLIN06 ne peuvent en aucun cas être le résultat d’une récupération spontanée chez les patients atteints de NOHL. » commente Bernard Gilly, Co-fondateur et Directeur Général de GenSight Biologics. « Nous avons l’intention d’apporter cette preuve scientifique parmi d’autres éléments aux autorités afin de construire un argumentaire solide et convaincant sur le bénéfice thérapeutique incontestable de LUMEVOQ®. »
LUMEVOQ® (GS010), la thérapie génique développée par GenSight Biologics pour le traitement de la perte de vision chez les patients atteints de NOHL associée à la mutation du gène mitochondrial ND4, doit faire l’objet d’une demande d’autorisation de mise sur le marché en Europe en septembre 2020.
L’analyse statistique de l’acuité visuelle chez les 23 sujets de l’étude REALITY présentant un gène ND4 muté a montré que, en moyenne, la vision ne s’améliorait pas après la chute brutale de la phase aigüe, et ce même des années après le début de la perte de vision. Cette détérioration brutale suivie d’une stabilisation de la faible acuité visuelle contraste avec les améliorations observées dans les études RESCUE et REVERSE de LUMEVOQ®.
Figure 1. Evolution de l’acuité visuelle chez les sujets de REALITY (âgés de 15 ans ou plus) présentant un gène ND4 muté et chez les sujets de RESCUE et REVERSE
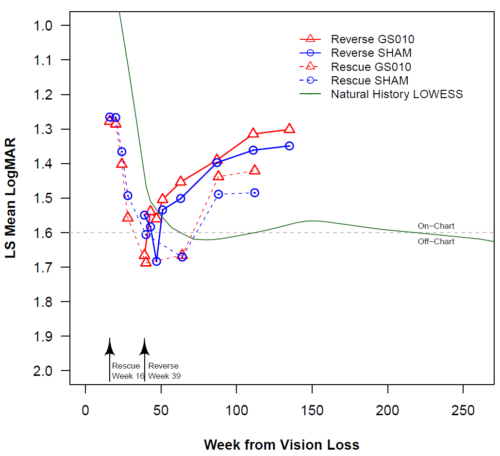
Remarque : BCVA = acuité visuelle (best-corrected visual acuity). La ligne LOWESS pour REALITY (n = 23 sujets âgés de 15 ans ou plus au début de la perte de vision) est basée sur une série de régressions polynomiales autour de chaque point de données. Les régressions utilisent un intervalle limité en arrière et en avant et donnent moins de poids aux points distants. L’évolution dans le temps de l’acuité visuelle pour REVERSE et RESCUE utilise la moyenne des moindres carrés basée sur une analyse de modèle mixte ANCOVA. Les points de départ des courbes sont définis sur la durée moyenne entre le début de la maladie et le moment du traitement (16 semaines pour RESCUE, 39 semaines pour REVERSE).
« Les résultats de REALITY sont entièrement conformes à une méta-analyse récente actuellement en cours de publication dans le Journal of Neuro-Ophthalmology *, qui montre que seulement environ 11% des patients atteints de NOHL ND4 présentent un certain degré d’amélioration spontanée significative de la vision. » déclare le Dr. Nancy J. Newman, Professeur d’Ophtalmologie et de Neurologie LeoDelle Jolley, Emory University School of Medicine, Atlanta, Géorgie, Etats-Unis, et l’un des plus grands spécialistes de la NOHL.
REALITY est une étude observationnelle rétrospective et transversale de sujets atteints de NOHL, menée dans des centres à travers l’Espagne, l’Italie, la France, le Royaume-Uni et les États-Unis. L’objectif est de générer des informations sur l’histoire naturelle de la maladie sur la base d’une approche qui faciliterait les comparaisons avec REVERSE et RESCUE. L’étude visait à inclure 50 sujets. Le recrutement a cependant dû être légèrement écourté en raison des mesures prises pour protéger les patients de la pandémie de COVID-19.
Sur les 44 sujets recrutés avant la mise en place des mesures COVID-19, 23 étaient âgés de 15 ans ou plus au moment de la perte de vision liée à la mutation de leur gène ND4. De ces 23 sujets ND4, 15 étaient traités par idebenone, dont la majorité dans les 12 premiers mois de perte de vision.
Les études pivots RESCUE et REVERSE ont évalué l’efficacité et la sécurité d’une injection intravitréenne unique de LUMEVOQ® chez des patients chez qui la perte d’acuité visuelle due à une NOHL associée à un gène mitochondrial ND4 muté avait débuté 0-6 mois et 6-12 mois avant le traitement, respectivement. 61 sujets des études RESCUE et REVERSE ont accepté de participer à l’étude de suivi à long-terme CLIN06, dont les premiers résultats ont récemment été publiés.
*N.J. Newman, V. Carelli, M. Taiel, P. Yu-Wai-Man. Visual outcomes in Leber hereditary optic neuropathy patients with the m. 11778>A (MTND4) mitochondrial DNA mutation. J Neuroophthalmol. En cours de publication (2020)
À propos de GenSight Biologics
GenSight Biologics S.A. (GenSight Biologics) est une société biopharmaceutique dédiée à la découverte et au développement de thérapies géniques innovantes pour le traitement des maladies neurodégénératives de la rétine et du système nerveux central. Le portefeuille de recherche de GenSight Biologics s’appuie sur deux plates-formes technologiques : le ciblage mitochondrial (Mitochondrial Targeting Sequence, ou MTS) et l’optogénétique, visant à préserver ou restaurer la vision chez les patients atteints de maladies neurodégénératives de la rétine. Le candidat médicament le plus avancé de GenSight Biologics, LUMEVOQ® (GS010), est en Phase III pour le traitement de la neuropathie optique héréditaire de Leber (NOHL), une maladie mitochondriale rare qui conduit à une perte irréversible de la vue chez les adolescents et les jeunes adultes. En utilisant son approche de thérapie génique, les candidats médicaments de GenSight Biologics sont destinés à offrir aux patients une récupération visuelle fonctionnelle durable après une seule injection intra-vitréenne dans chaque œil.
À propos de LUMEVOQ® (GS010)
LUMEVOQ® (GS010) cible la neuropathie optique héréditaire de Leber (NOHL), et s’appuie sur une technologie propriétaire de séquence de ciblage mitochondrial (MTS), issue des travaux de l’Institut de la Vision, qui, lorsqu’elle est associée au gène d’intérêt, permet de l’adresser spécifiquement à l’intérieur de la mitochondrie grâce à un vecteur AAV (Adeno-Associated Virus). Le gène d’intérêt est ainsi transféré dans la cellule pour y être exprimé et produire la protéine fonctionnelle, qui sera acheminée à l’intérieur des mitochondries grâce aux séquences nucléotidiques spécifiques, afin de restaurer la fonction mitochondriale déficiente ou manquante. « LUMEVOQ » a été autorisé comme nom commercial pour le GS010 (lenadogene nolparvovec) par l’Agence Européenne du Médicament (EMA) en octobre 2018.
À propos de la Neuropathie Optique Héréditaire de Leber (NOHL)
La neuropathie optique héréditaire de Leber (NOHL) est une maladie mitochondriale rare, de transmission maternelle, caractérisée par une dégénérescence des cellules ganglionnaires de la rétine et provoquant en moins d’un an une perte brutale et irréversible de la vision conduisant généralement à la cécité légale. Ces symptômes apparaissent principalement chez les adolescents et les jeunes adultes. La NOHL provoque une perte brutale, soudaine et sans douleur de la vision centrale dans le 1er œil, puis le 2nd œil est atteint à son tour, de manière irréversible. 97% des patients présentent une perte bilatérale de la vision en moins d’un an, et cette perte de vision est simultanée dans 25% des cas. La NOHL causerait la cécité visuelle chez environ 1 200 personnes par an aux Etats-Unis et en Europe.
À propos de RESCUE et REVERSE
RESCUE et REVERSE sont deux études distinctes de Phase III randomisées, en double masqué, contrôlées par injection simulée (sham), conçues pour évaluer l’efficacité d’une injection intravitréenne unique de GS010 (rAAV2/2-ND4) chez des sujets atteints de la NOHL induite par la mutation G11778A ND4.
Le critère d’évaluation principal mesurera la différence d’efficacité de GS010 entre les yeux traités et les yeux non-traités (sham), sur la base de l’acuité visuelle (Best Corrected Visual Acuity ou BCVA), mesurée à l’aide de l’échelle ETDRS à 48 semaines après injection. Les scores « Logarithm of the Minimal Angle of Resolution » des patients, ou LogMAR, qui sont dérivés du nombre de lettres lues sur l’échelle ETDRS, seront utilisés à des fins statistiques. Les deux études ont été conçues pour évaluer une différence statistiquement significative d’au moins 15 lettres ETDRS entre les yeux traités et non-traités (sham), ajustés de l’acuité visuelle initiale (baseline).
Les critères d’évaluation secondaires incluront l’application de l’analyse principale aux yeux ayant reçu GS010 et présentant à l’inclusion la meilleure acuité visuelle initiale (« meilleur œil »), comparés à ceux ayant reçu la procédure sham, ainsi qu’aux yeux ayant reçu GS010 et présentant la moins bonne acuité visuelle initiale (« moins bon œil »), comparés à ceux ayant reçu la procédure sham. Également, une évaluation de la proportion de patients « répondeurs » sera réalisée, incluant notamment le pourcentage de patients qui maintiennent leur acuité visuelle (perte de moins de 15 lettres ETDRS), le pourcentage de patients qui améliorent leur acuité visuelle de 15 lettres ETDRS ou plus, ainsi que le pourcentage de patients présentant une acuité visuelle finale >20/200, ou 1/10. Les paramètres visuels mesurés incluront également les champs visuels automatisés, la tomographie par cohérence optique, ainsi que la sensibilité aux couleurs et aux contrastes, en plus des mesures de qualité de vie, de bio-dissémination, et de réponse immunitaire post-injection.
Les études sont actuellement menées en parallèle, chez 37 patients pour REVERSE et 39 patients pour RESCUE, dans 7 centres aux États-Unis, au Royaume-Uni, en France, en Allemagne et en Italie. Les résultats à 96 semaines de suivi des deux études ont été publiés en 2019. Les patients ont ensuite été transférés vers une étude de suivi à long terme pour 3 années supplémentaires.
Identifiants ClinicalTrials.gov :
REVERSE : NCT02652780
RESCUE : NCT02652767
À propos de CLIN06 (suivi à long terme des études RESCUE et REVERSE)
CLIN06 est une étude de suivi à long terme de sujets atteints de NOHL ND4 traités avec la thérapie génique LUMEVOQ® (GS010) dans le cadre des études cliniques de Phase III RESCUE ou REVERSE. La durée totale de l’étude de suivi est de 3 ans, soit 5 ans après l’injection. Aucun traitement de l’étude n’est administré pendant le suivi de CLIN06.
L’objectif principal est d’évaluer la sécurité à long terme d’une injection intravitréenne de LUMEVOQ® jusqu’à 5 ans après le traitement. L’objectif secondaire est d’évaluer l’efficacité à long terme du traitement ainsi que la qualité de vie des sujets pendant 5 ans après le traitement. Le premier sujet a été recruté le 9 janvier 2018, et 61 sujets ont été recrutés.
Identifiants ClinicalTrials.gov :
CLIN06 : NCT03406104
À propos de REALITY
REALITY est une étude observationnelle rétrospective et transversale internationale de sujets atteints de NOHL, basée sur les dossiers médicaux et l’administration d’enquêtes sur la qualité de vie liée à la santé (HRQoL), ainsi que les coûts directs et indirects associés à la maladie.
L’étude vise à recruter au moins 50 sujets (adultes et pédiatriques) principalement dans les pays suivants : Espagne, Italie, France, Royaume-Uni et États-Unis.
Les principaux objectifs de l’étude REALITY sont les suivants : décrire l’évolution des changements fonctionnels et structurels visuels, ainsi que d’autres symptômes associés chez les patients atteints de NOHL ; comprendre l’impact de la perte de vision liée à la NOHL sur la HRQoL ; et comprendre les impacts économiques pour les patients et leurs familles découlant des coûts directs et indirects associés à la maladie. L’objectif secondaire est de décrire la relation entre les facteurs génétiques, de style de vie et / ou environnementaux et l’expression du phénotype NOHL.
Le premier sujet a été recruté le 3 janvier 2018, et le recrutement a pris fin au début du second trimestre 2020.
Identifiants ClinicalTrials.gov :
REALITY LHON Registry: NCT03295071
Contacts
-
LifeSci AdvisorsRelations InvestisseursGuillaume van Renterghem+41 (0)76 735 01 31
-
Orpheon FinanceInvestisseurs ParticuliersJames Palmer+33 7 60 92 77 74