- Amélioration durable de l’acuité visuelle, les yeux traités par GS010 obtenant une amélioration de +15,4 lettres ETDRS par rapport à l’inclusion et une amélioration de +28,1 lettres ETDRS par rapport au nadir
- L’amélioration bilatérale des principales mesures de la fonction visuelle, l’acuité visuelle (BCVA) et la sensibilité aux contrastes, se poursuit
- Les analyses de répondeurs suggèrent une amélioration des paramètres cliniques des yeux traités par GS010 par rapport aux yeux sham
- Sécurité et tolérance de GS010 établies au cours de l’étude
- Dossier d’information intégrant les résultats en préparation pour rencontrer les autorités réglementaires
Paris, France, mercredi 15 mai 2019, 7h30 CEST – GenSight Biologics (Euronext : SIGHT, ISIN : FR0013183985, éligible PEA-PME), société biopharmaceutique dédiée à la découverte et au développement de thérapies géniques innovantes pour le traitement des maladies neurodégénératives de la rétine et du système nerveux central, annonce aujourd’hui un premier ensemble de résultats de la semaine 96 de l’étude clinique de Phase III REVERSE. L’étude a évalué la sécurité et l’efficacité d’une seule injection intravitréenne de GS010 (rAAV2/2-ND4) chez 37 patients atteints de neuropathie optique héréditaire de Leber (NOHL) induite par la mutation 11778-ND4 et chez qui la perte d’acuité visuelle a débuté entre 6 et 12 mois avant le traitement. La semaine 96 correspond à la dernière annonce programmée de résultats de l’étude, et au moment de la levée du masque qui donnera accès aux profils des patients individuels.
Les résultats témoignent de l’efficacité continue de GS010 deux ans après l’injection, avec le maintien d’une amélioration cliniquement significative de l’acuité visuelle (best-corrected visual acuity, BCVA) par rapport à la baseline. À la semaine 96, les yeux traités par GS010 ont montré une amélioration moyenne de -0,308 LogMAR par rapport à l’inclusion, correspondant à +15,4 lettres ETDRS ou 3 lignes ETDRS. Ce niveau cliniquement significatif d’amélioration de l’acuité visuelle maintient le gain observé à la semaine 72 (+14,7 lettres ETDRS).
Comme observé dans les résultats précédents (semaine 48 et semaine 72), l’acuité visuelle dans les yeux sham (yeux non traités, ayant reçu une injection simulée) a évolué selon une trajectoire relativement parallèle, montrant une amélioration moyenne de -0,259 LogMAR par rapport à la baseline, soit un gain de +12,9 lettres ETDRS, à la semaine 96. Bien que d’ampleur plus faible, l’amélioration moyenne de l’acuité visuelle dans les yeux sham n’a pas montré de différence statistiquement significative par rapport aux yeux traités par GS010.
Figure 1 : Amélioration bilatérale prolongée de l’acuité visuelle
(best-corrected visual acuity, BCVA) dans REVERSE
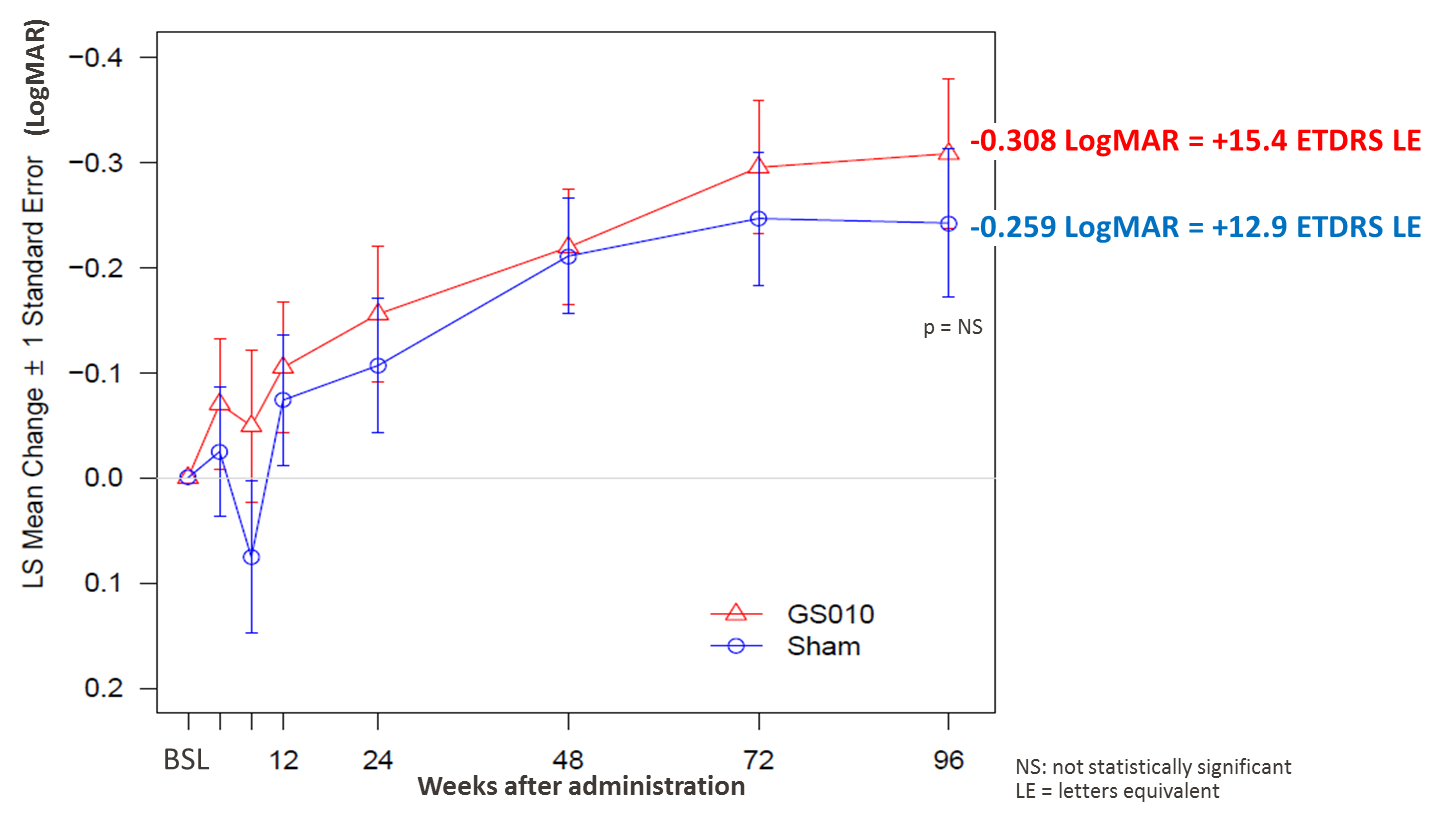
Remarques : Un modèle mixte d’analyse de covariance (ANCOVA) a été utilisé avec la variation par rapport à la baseline comme réponse, et le sujet et les yeux du patient comme facteurs aléatoires, le traitement et la valeur LogMAR à la baseline comme covariables dans le modèle.
Comme dans RESCUE, et cohérent avec l’histoire naturelle, les patients ont présenté un point bas de l’acuité visuelle, ou nadir. Les yeux des patients de REVERSE ont montré une récupération remarquable. À la semaine 96, les yeux traités par GS010 avaient récupéré +28 lettres par rapport à leur nadir.
Tableau 1. Récupération de l’acuité visuelle par rapport au nadir* : RESCUE et REVERSE (Différence** par rapport au nadir* en lettres ETDRS, moyenne et écart type)
| RESCUE | REVERSE | ||||||
| n | Semaine 48 | Semaine 72 | n | Semaine 48 | Semaine 72 | Semaine 96 | |
| Yeux traités par GS010 | 34 | +12,9
(17,9) |
+20,6
(26,4) |
37 | +24,1
(21,1) |
+27,4
(21,8) |
+28,1
(22,0) |
| Yeux sham | 33 | +11,8
(16,0) |
+21,8
(25,1) |
37 | +20,3
(23,4) |
+22,6
(25,5) |
+23,2
(24,5) |
Remarque : *Le nadir a été défini comme l’acuité visuelle en LogMAR après traitement la plus faible jusqu’à la semaine d’intérêt. La vision LP/NLP (perception de la lumière [Light Perception, LP] / absence de perception de la lumière [No Light Perception, NLP] n’a pas été incluse dans l’analyse. **La variation par rapport au nadir a d’abord été calculée en utilisant les valeurs LogMAR observées ; aucune donnée n’a été imputée. Les valeurs LogMAR ont ensuite été converties en lettres ETDRS.
À la semaine 96, une seconde mesure essentielle de la fonction visuelle — la sensibilité aux faibles contrastes, mesurée par l’échelle de Pelli-Robson — a montré une tendance à l’amélioration similaire à la fois pour les yeux traités par GS010 et pour les yeux sham.
Figure 2 : Évolution de la sensibilité aux contrastes dans REVERSE
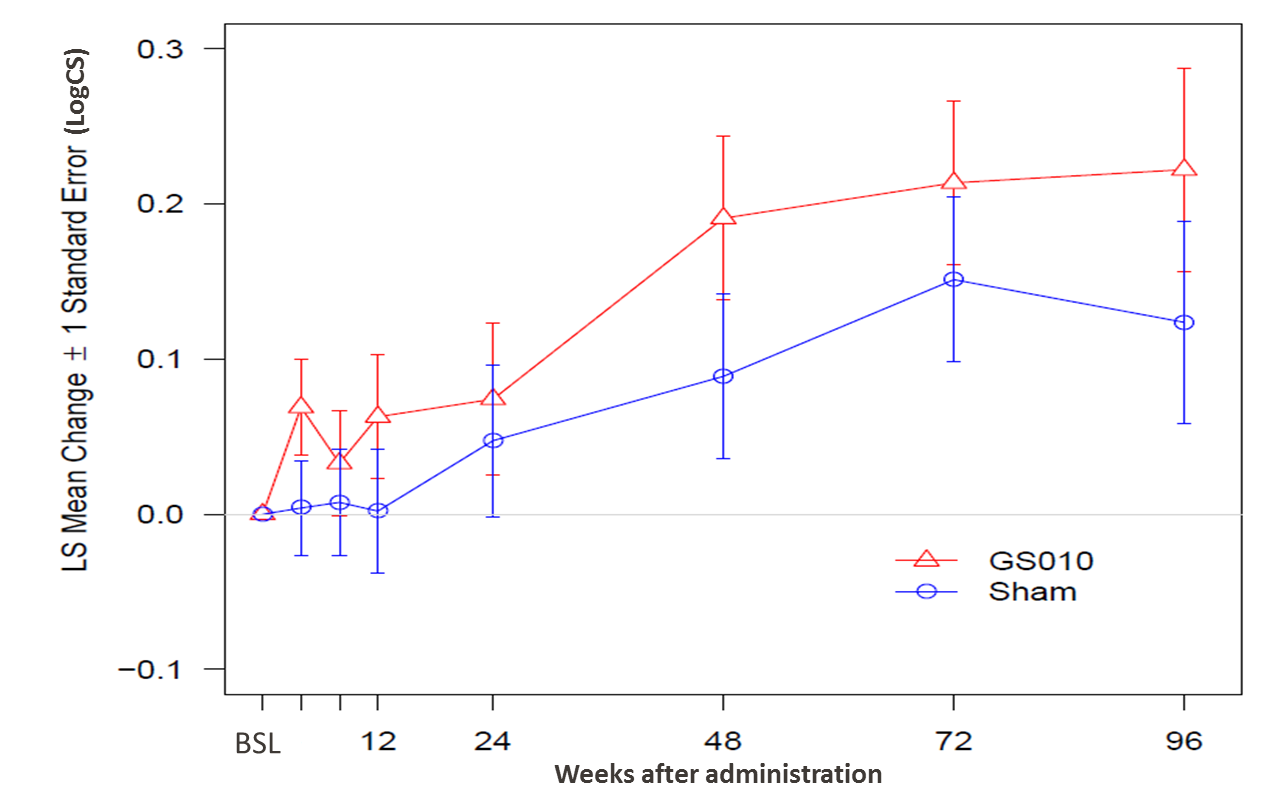
Remarques : Un modèle mixte d’analyse de covariance (ANCOVA), avec des mesures répétées pour l’œil et un ajustement par covariable de la baseline en LogCS, a été utilisé pour modéliser l’effet du traitement sur la variation en LogCS par rapport à la baseline. Une analyse séparée a été conduite à chaque mesure dans le temps.
La sensibilité aux contrastes n’a toutefois pas suivi une trajectoire aussi parallèle que celle de l’acuité visuelle : la sensibilité aux contrastes moyenne pour les yeux traités par GS010 montre une amélioration plus robuste par rapport à la baseline au cours de l’étude. Quoi qu’il en soit, la baisse de la sensibilité aux contrastes moyenne des yeux sham n’a pas été suffisante pour générer une différence statistiquement significative de l’amélioration de la sensibilité aux contrastes moyenne à la semaine 96 entre les deux groupes d’yeux.
« Les données indiquent que les yeux traités comme les yeux sham montrent une amélioration à la fois des contrastes élevés et des faibles contrastes, défiant et surpassant l’histoire naturelle acceptée de cette maladie, basée sur les expériences cliniques de générations de neuro-ophtalmologistes », a commenté le Dr Robert C. Sergott, directeur, Wills Eye Hospital, Neuro-Ophtalmologie, et directeur, William H. Annesley, Jr, EyeBrain Center, Université Thomas Jefferson, Philadelphie, Pennsylvanie, États-Unis. « Le comportement de l’œil non traité doit également nous conduire à réexaminer ce que nous pensions être un dogme, et à nous ouvrir à l’idée que la thérapie génique délivrée dans un œil pourrait accéder à l’œil controlatéral. »
« Il est encourageant que les yeux traités par GS010 aient eu une probabilité d’atteindre une vision supérieure à 20/200 près de 4 fois plus élevée que les yeux sham. La prochaine étape, qui est d’analyser les données longitudinales individuelles sur les paramètres visuels de chaque patient recruté dans REVERSE, devrait encore clarifier le bénéfice thérapeutique du GS010 dans la NOHL induite par la mutation 11778-ND4 », a indiqué le Dr Patrick Yu-Wai Man, maître de conférences et consultant honoraire en ophtalmologie à l’Université de Cambridge, au Moorfields Eye Hospital et à l’UCL Institute of Ophthalmology, Londres, Royaume-Uni.
Une autre analyse de répondeurs fournit une perspective intéressante sur les résultats de REVERSE. Dans une étude d’histoire naturelle de la maladie conduite par Santhera1, 15 % des patients porteurs de la mutation 11778A ont obtenu une « récupération cliniquement pertinente » (clinically relevant recovery, CRR), définie comme suit, dans au moins un œil :
- Amélioration d’au moins 10 lettres ETDRS de leur acuité visuelle, ou
- Amélioration d’un niveau d’acuité visuelle off-chart à la possibilité de lire au moins 5 lettres ETDRS (on-chart)
À titre de comparaison, 68% des patients de REVERSE ont obtenu une CRR selon cette définition à la semaine 96, les yeux traités par GS010 ayant une probabilité significativement plus élevée d’obtenir cette CRR que les yeux sham (62% contre 43%, p = 0,0348).
Les améliorations de la fonction visuelle se reflètent dans les scores de qualité de vie (Visual Function Questionnaire-25, VFQ-25) du National Eye Institute (NEI), un questionnaire validé de qualité de vie liée à la vision complété par les patients de REVERSE. Le score composite moyen et les scores moyens aux sous-échelles pertinentes ont continué à s’améliorer par rapport à la baseline, en particulier concernant la capacité à accomplir les activités avec vision de près et les activités avec vision de loin. L’augmentation des scores moyens aux sous-échelles par rapport à la baseline a dépassé celles associées à une amélioration de 15 lettres de la BCVA dans d’autres malades oculaires.
Tableau 2 : Améliorations significatives des scores de qualité de vie rapportées par les patients de REVERSE
Résultats au questionnaire NEI VFQ-25 dans REVERSE
Variation moyenne par rapport à la baseline (en score absolu et en pourcentage)
| Score composite** | Activités avec vision de près | Activités avec vision de loin | Dépendance | Limites fonctionnelles | Vision générale | Santé mentale | |
| Semaine 48 | +7,2
+23,2 % |
+10,4
+65,1 % |
+9,6
+49,8 % |
+12,4
+100,6 % |
+14,5
+65,0 % |
+10,3
+50,9 % |
+11,2
+81,9 % |
| Semaine 72 | +8,1
+25,2 % |
+9,5
+58,1 % |
+8,2
+42,5 % |
+18,9
+130,2 % |
+15,2
+70,9 % |
+11,9
+54,1 % |
+15,2
+105,6 % |
| Semaine 96 | +9,5
+28,8 % |
+13,3
+78,1 % |
+10,7
+47,4 % |
+18,5
130,2 % |
+15,9
+78,9 % |
+6,5
+32,4 % |
+16,1
+108,2 % |
| Différence cliniquement pertinente* | +3,90 à +4,34 | +4,67 à +6,06 | +5,15 à +5,38 | +4,72 à +4,98 | +3,31 à +4,70 | +4,38 à +4,82 | +4,70 à +4,88 |
*Suñer et al. (2009) : différences entre les scores cliniquement pertinentes basées sur une amélioration cliniquement significative de la BCVA de 15 lettres à 12 mois.
**Le score composite est une moyenne des scores aux sous-échelles ciblant la vision, à l’exclusion de la question sur la santé générale.
Remarque : L’amélioration moyenne en pourcentage pour un sous-score a été calculée en établissant la moyenne des améliorations individuelles en pourcentage.
Les mesures structurelles indiquent que les yeux traités par GS010 ont maintenu la stabilité observée précédemment concernant le volume des cellules ganglionnaires. L’effet différentiel du traitement était toutefois plus important lors des résultats précédents.
Les analyses des données individuelles des sujets suggèrent que l’effet bilatéral est courant chez les patients. D’autres analyses des données individuelles de REVERSE sont en cours. GenSight tiendra une réunion investisseurs le 23 mai à New York, lors de laquelle des Key Opinion Leaders reconnus commenteront les résultats en détails (en anglais, traduction simultanée en français).
Les données à 96 semaines confirment le profil de sécurité favorable de GS010. Il n’y a eu aucune sortie de l’étude et aucun effet indésirable grave dans les yeux traités par GS010. Les évènements indésirables (EI) oculaires les plus fréquemment rapportés dans le groupe traité ont été principalement liés à la procédure d’injection elle-même, en plus de la survenue d’une inflammation intraoculaire (s’accompagnant d’une élévation de la pression intraoculaire chez certains patients), probablement liée à GS010 ; ces cas ont répondu au traitement conventionnel et ne se sont accompagnés d’aucune séquelle.
« Nous sommes très heureux de ces résultats remarquables, qui démontrent l’effet durable et cliniquement significatif du GS010, tout en confirmant la sécurité de notre thérapie génique », a commenté Bernard Gilly, co-fondateur et directeur général de GenSight. « Nous progressons avec vitesse et détermination pour constituer un dossier robuste à partir des résultats de REVERSE et, plus tard dans le courant de l’année, de RESCUE. »
Les résultats de REVERSE à la semaine 96 seront inclus dans les matériels d’information en cours de préparation pour une réunion de pré-soumission avec l’EMA et une réunion Type B avec la FDA, les deux étant prévues pour le milieu de l’année.
Les résultats à 96 semaines de la deuxième étude de Phase III de GS010, RESCUE, devraient être annoncés d’ici la fin du troisième trimestre 2019.
La troisième étude interventionnelle de GS010, REFLECT, est un essai de Phase III randomisé, en double masqué et contrôlé par placebo, qui vise à évaluer la sécurité et l’efficacité d’injections bilatérales de GS010 chez les patients ayant perdu la vue depuis moins d’un an des suites de la NOHL. Le premier patient de REFLECT a été traité en mars 2018, et le dernier patient devrait être inclus au second trimestre 2019.
GenSight tiendra une conférence téléphonique aujourd’hui, 15 mai 2019, à 10h00 CEST en français et à 14h30 CEST (8h30 EST) en anglais, afin de discuter ces résultats.
Webcast & Conférence téléphonique en français
Numéros de la conférence téléphonique :
- États-Unis : +1 212 999 6659
- France : +33 (0) 1 7037 7166
- Royaume-Uni : +44 (0) 20 3003 2666
- Mot de passe : GenSight
Lien Webcast : https://channel.royalcast.com/webcast/gensightbiologicsfr/20190514_1/
Webcast & Conférence téléphonique en anglais
Numéros de la conférence téléphonique :
- États-Unis : +1 212 999 6659
- France : +33 (0) 1 7037 7166
- Royaume-Uni : +44 (0) 20 3003 2666
- Mot de passe : GenSight
Lien Webcast : https://channel.royalcast.com/webcast/gensightbiologicsen/20190514_1/
Une rediffusion de la conférence téléphonique et du webcast sera disponible en utilisant les liens ci-dessus.
Référence :
- Magda et al (2019), “Natural History of Leber’s Hereditary Optic Neuropathy (LHON): Findings from a Large Patient Cohort”, Poster présenté au NANOS, 16-21 mars 2019 ; Poster Session II: Scientific Advancements; Poster: 163
À propos de GenSight Biologics
GenSight Biologics S.A. (GenSight Biologics) est une société biopharmaceutique dédiée à la découverte et au développement de thérapies géniques innovantes pour le traitement des maladies neurodégénératives de la rétine et du système nerveux central. Le portefeuille de recherche de GenSight Biologics s’appuie sur deux plates-formes technologiques : le ciblage mitochondrial (Mitochondrial Targeting Sequence, ou MTS) et l’optogénétique, visant à préserver ou restaurer la vision chez les patients atteints de maladies neurodégénératives de la rétine. Le candidat médicament le plus avancé de GenSight Biologics, GS010, est en Phase III pour le traitement de la neuropathie optique héréditaire de Leber (NOHL), une maladie mitochondriale rare qui conduit à une perte irréversible de la vue chez les adolescents et les jeunes adultes. En utilisant son approche de thérapie génique, les candidats médicaments de GenSight Biologics sont destinés à offrir aux patients une récupération visuelle fonctionnelle durable après une seule injection intra-vitréenne dans chaque œil.
À propos de GS010
GS010 cible la neuropathie optique héréditaire de Leber (NOHL), et s’appuie sur une technologie propriétaire de séquence de ciblage mitochondrial (MTS), issue des travaux de l’Institut de la Vision, qui, lorsqu’elle est associée au gène d’intérêt, permet de l’adresser spécifiquement à l’intérieur de la mitochondrie grâce à un vecteur AAV (Adeno-Associated Virus). Le gène d’intérêt est ainsi transféré dans la cellule pour y être exprimé et produire la protéine fonctionnelle, qui sera acheminée à l’intérieur des mitochondries grâce aux séquences nucléotidiques spécifiques, afin de restaurer la fonction mitochondriale déficiente ou manquante.
À propos de la Neuropathie Optique Héréditaire de Leber (NOHL)
La neuropathie optique héréditaire de Leber (NOHL) est une maladie mitochondriale rare, de transmission maternelle, caractérisée par une dégénérescence des cellules ganglionnaires de la rétine et provoquant en moins d’un an une perte brutale et irréversible de la vision conduisant généralement à la cécité légale. Ces symptômes apparaissent principalement chez les adolescents et les jeunes adultes. La NOHL provoque une perte brutale, soudaine et sans douleur de la vision centrale dans le 1er œil, puis le 2nd œil est atteint à son tour, de manière irréversible. 97% des patients présentent une perte bilatérale de la vision en moins d’un an, et cette perte de vision est simultanée dans 25% des cas. La NOHL causerait la cécité visuelle chez environ 1 400 à 1 500 personnes par an aux Etats-Unis et en Europe.
À propos de RESCUE et REVERSE
RESCUE et REVERSE sont deux études distinctes de Phase III randomisées, en double masqué, contrôlées par injection simulée (sham), conçues pour évaluer l’efficacité d’une injection intravitréenne unique de GS010 (rAAV2/2-ND4) chez des sujets atteints de la NOHL induite par la mutation G11778A ND4.
Le critère d’évaluation principal mesurera la différence d’efficacité de GS010 entre les yeux traités et les yeux non-traités (sham), sur la base de l’acuité visuelle (Best Corrected Visual Acuity ou BCVA), mesurée à l’aide de l’échelle ETDRS à 48 semaines après injection. Les scores « Logarithm of the Minimal Angle of Resolution » des patients, ou LogMAR, qui sont dérivés du nombre de lettres lues sur l’échelle ETDRS, seront utilisés à des fins statistiques. Les deux études ont été conçues pour évaluer une différence statistiquement significative d’au moins 15 lettres ETDRS entre les yeux traités et non-traités (sham), ajustés de l’acuité visuelle initiale (baseline).
Les critères d’évaluation secondaires incluront l’application de l’analyse principale aux yeux ayant reçu GS010 et présentant à l’inclusion la meilleure acuité visuelle initiale (« meilleur œil »), comparés à ceux ayant reçu la procédure sham, ainsi qu’aux yeux ayant reçu GS010 et présentant la moins bonne acuité visuelle initiale (« moins bon œil »), comparés à ceux ayant reçu la procédure sham. Également, une évaluation de la proportion de patients « répondeurs » sera réalisée, incluant notamment le pourcentage de patients qui maintiennent leur acuité visuelle (perte de moins de 15 lettres ETDRS), le pourcentage de patients qui améliorent leur acuité visuelle de 15 lettres ETDRS ou plus, ainsi que le pourcentage de patients présentant une acuité visuelle finale >20/200, ou 1/10. Les paramètres visuels mesurés incluront également les champs visuels automatisés, la tomographie par cohérence optique, ainsi que la sensibilité aux couleurs et aux contrastes, en plus des mesures de qualité de vie, de bio-dissémination, et de réponse immunitaire post-injection.
Les études sont actuellement menées en parallèle, chez 37 patients pour REVERSE et 39 patients pour RESCUE, dans 7 centres aux États-Unis, au Royaume-Uni, en France, en Allemagne et en Italie. Les résultats à 96 semaines de suivi des deux études sont attendus en 2019. Les patients seront ensuite transférés vers une étude de suivi à long terme pour 3 années supplémentaires.
Identifiants ClinicalTrials.gov :
REVERSE : NCT02652780
RESCUE : NCT02652767
À propos de REFLECT
REFLECT est une étude multicentrique, randomisée, en double aveugle, contrôlée contre placebo visant à évaluer l’innocuité et l’efficacité des injections bilatérales de GS010 chez des sujets atteints par la LHON en raison de la mutation NADH déshydrogénase 4 (ND4).
L’essai prévoit de recruter 90 patients présentant un début de perte de vision d’une durée d’un an et qui sera mené dans plusieurs centres en Europe et aux États-Unis.
Dans le bras actif, GS010 sera administré en une seule injection intravitréenne aux deux yeux de chaque sujet. Dans le bras placebo, GS010 sera administré en une seule injection intravitréenne au premier œil affecté, tandis que l’autre œil recevra une injection placebo.
Le critère d’évaluation principal de l’étude REFLECT est la BCVA signalée dans LogMAR après un an de traitement dans le deuxième œil affecté / non encore affecté. Le changement par rapport aux valeurs initiales chez les deuxièmes yeux affectés / non encore affectés recevant GS010 et le placebo sera la principale réponse d’intérêt. Les critères d’efficacité secondaires incluent : BCVA reporté dans LogMAR à 2 ans après le traitement dans le deuxième œil affecté / non encore affecté par rapport au placebo et au premier œil affecté recevant GS010, PTOM, sensibilité aux couleurs et au contraste et échelles de qualité de vie. Le premier patient a été traité en mars 2018.
Identifiants ClinicalTrials.gov :
REFLECT: NCT03293524
Contacts
-
Orpheon FinanceInvestisseurs ParticuliersJames Palmer+33 7 60 92 77 74